per Laura Arribas Ruscalleda
Aquests últims anys la paraula “virus” ha ressonat i impactat en les nostres vides d’una manera més que notable, però què sabem realment sobre els virus? Quant temps fa que estan entre nosaltres? Són els nostres enemics? Tantes són les preguntes que ens podem arribar a fer sobre aquests patògens microscòpics que és difícil saber per on començar. Per intentar resoldre’n alguna us explicaré una història, la història de com els virus podrien salvar-nos la vida.
Possibles aliats en la foscor
No hi ha dubte que la percepció tant per part de la població com de la comunitat científica cap als virus ha estat sempre associada a males notícies, però a començaments del segle XX una petita guspira va iniciar el canvi de paradigma amb el descobriment dels bacteriòfags.
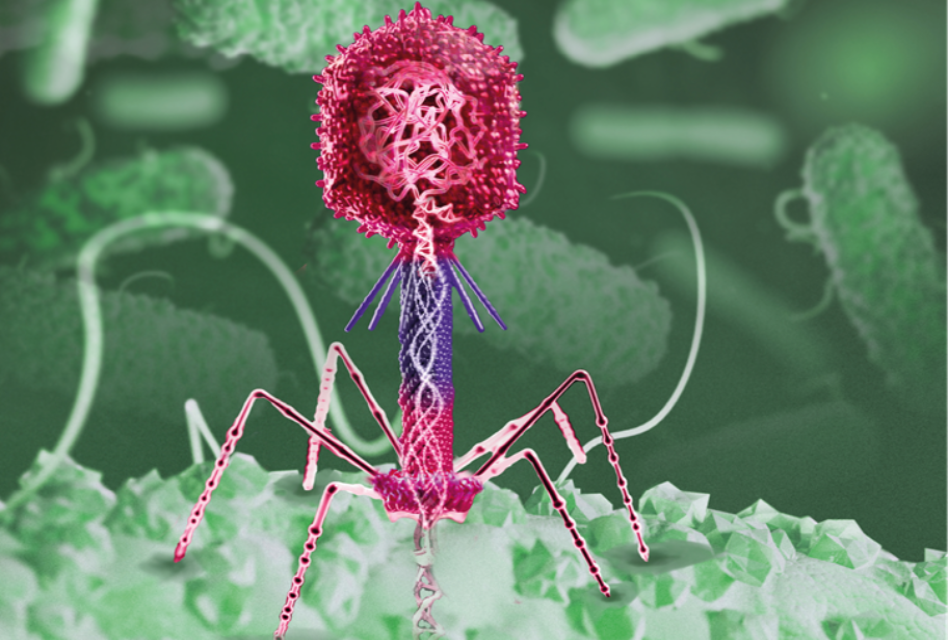
Els bacteriòfags son virus que infecten i es repliquen en bacteris, uns dels nostres altres grans enemics microscòpics, que van ser descoberts pel microbiòleg francès Félix d’Hérelle. L’estructura dels bacteriòfags està composta per una càpsida proteica, que conté el seu material genètic, unida a una cua que acaba en una estructura que fan servir per unir-se a la superfície del bacteri i que anomenem aparell d’adsorció.
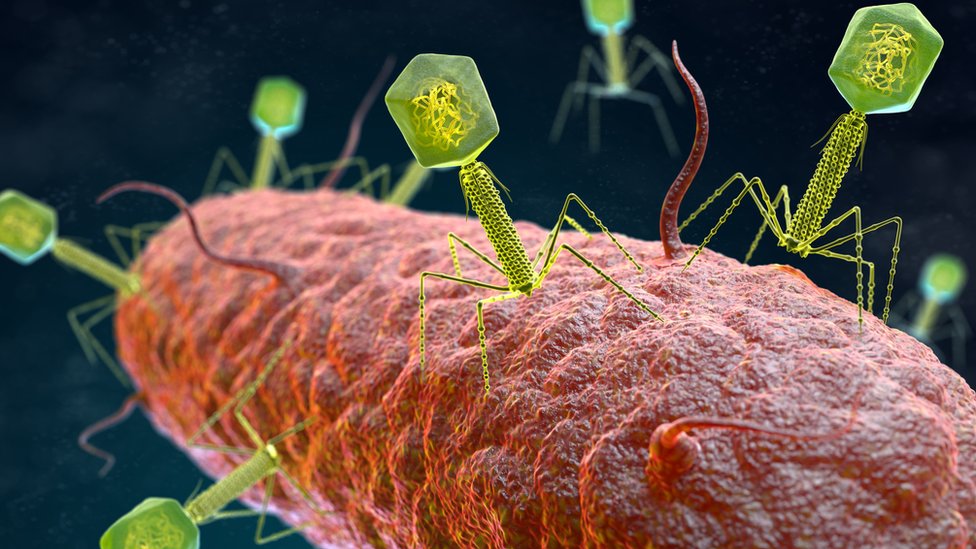
D’Hérelle va proposar la teràpia amb bacteriòfags per tractar infeccions bacterianes humanes i animals durant la Primera Guerra Mundial. Tanmateix, la reticència occidental davant l’enfocament de la teràpia proposada pel microbiòleg i el posterior descobriment dels antibiòtics van provocar que la recerca sobre els bacteriofags s’allunyés del camí que ell havia plantejat.
Els antibiòtics van suposar un abans i un després per al control de les malalties infeccioses, ja que gràcies a la seva implementació com a tractament antibacterià s’han salvat milions de vides. Actualment, ens trobem en un període d’elevada amenaça davant els bacteris resistents als antibiòtics. Tot i que la resistència als antibiòtics en bacteris humans existia prèviament al descobriment d’aquests fàrmacs, la seva prevalença era baixa. En l’actualitat la situació és molt diferent i ja parlem de 4,7 milions de morts el 2021, i es calcula que aquesta xifra ascendiria als 8,2 milions el 2050.
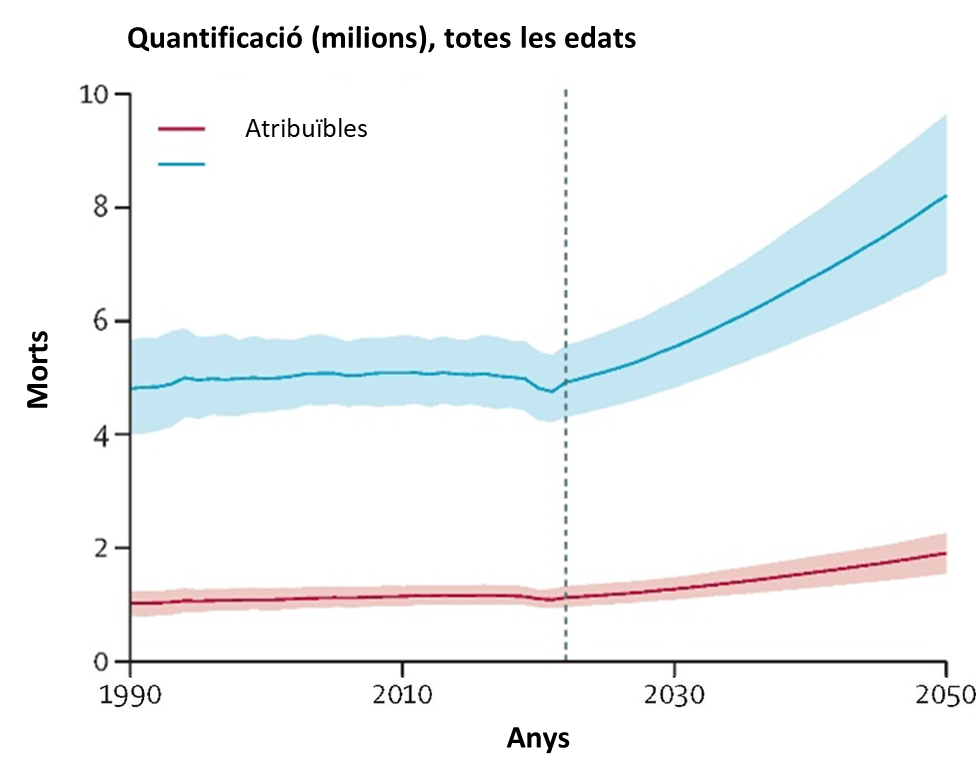
Ens espera un futur desprotegit de les infeccions bacterianes?
Aquells que ens dediquem a la virologia, de manera paradoxal, ens sentim atrets pels secrets que s’amaguen en el cicle viral d’aquests organismes. Ha estat aquesta fascinació pel funcionament detallat dels virus la que ha permès descobrir el seu potencial terapèutic, sovint ocult rere la percepció negativa que se’n té. Els bacteriòfags són un clar exemple d’aquest potencial terapèutic.
Els virus són agents infecciosos acel·lulars que utilitzen la maquinària molecular dels organismes que infecten per poder replicar-se i així continuar infectant altres organismes successivament. Els virus que infecten els bacteris són els bacteriòfags, que han coevolucionat amb ells durant gairebé 4.000 milions d’anys. A causa d’això, sabem que cada bacteriòfag presenta un rang d’hostes concrets que pot atacar, el qual pot ser ampli (pot infectar moltes espècies dins d’un gènere bacterià i, de vegades, en diferents gèneres) o més restringit (pot infectar només un o un petit nombre d’aïllats dins d’una espècie bacteriana).
També és important destacar que els bacteriòfags són els organismes més abundants del planeta, per la qual cosa hi ha un ventall molt ampli de varietat. Es localitzen de manera natural en pràcticament qualsevol nínxol del planeta on es trobin bacteris; per exemple el sòl, l’aigua i una gran varietat de productes alimentaris.
Per tal de poder eliminar els bacteris, els bacteriòfags s’adhereixen a la superfície bacteriana mitjançant el seu aparell d’adsorció per poder introduir el seu material genètic en l’interior del bacteri. Gràcies a les eines moleculars del bacteri hoste, se sintetitzaran les proteïnes i el material genètic necessaris per a la producció de nous bacteriòfags que ocasionaran la lisi del bacteri, és a dir, la seva destrucció.
Una de les vies de recerca per aconseguir un bacteriòfag que compleixi amb els nostres interessos, és a dir, que infecti selectivament al bacteri al qual es vol atacar, es podria comparar amb la recerca d’un tresor, ja que es realitza mostreig en aigües, sòl, fang i superfícies biòtiques.
En cas que no disposem de cap bacteriòfag capaç de combatre un bacteri concret existeixen alternatives com l’evolució dirigida per facilitar el desenvolupament d’un bacteriòfag especialitzat contra un bacteri, o directament la creació sintètica de nous bacteriòfags.
La teràpia amb bacteriòfags ha experimentat un creixement considerable en la seva possible aplicació clínica, amb un augment dels assaigs clínics actius en els últims anys, especialment des de l’inici de 2020. Els programes de teràpia amb bacteriòfags estan establerts als Estats Units, Bèlgica, França, Suècia, així com a la República de Geòrgia i Polònia, i han tingut èxit en el desenvolupament de protocols estàndard per a la seva aplicació terapèutica.
Tot i que els bacteriòfags es consideren generalment ben tolerats en humans i animals, la seva administració presenta certs reptes segons la via de distribució, com és el cas de les infeccions entèriques o pulmonars, que requereixen formulacions específiques per assegurar la seva viabilitat i estabilitat. Així doncs, la recerca actual se centra en l’optimització de l’administració de bacteriòfags, incloent-hi la seva combinació amb antibiòtics per aconseguir un tractament més eficaç, especialment en infeccions resistents als antibiòtics.
Ja per acabar…
L’ús de bacteriòfags com a teràpia encara continua en fase d’estudi, ja que són moltes les variables a tenir en compte per a la seva aprovació com a tractament. Malgrat això, actualment es permet la seva aplicació com a teràpia per a ús compassiu en pacients amb qui les opcions de tractament amb antibiòtics han fallat, mostrant resultats molt prometedors. L’objectiu de la teràpia amb bacteriòfags no és desbancar als antibiòtics de la seva posició, sinó fer-los servir d’aliats contra els bacteris, com a tractament complementari.
Aquest és només un dels casos en què els virus, actualment, s’estan utilitzant com a eina a favor nostre per abordar problemes biomèdics. Igual que quan parlem de literatura no podem jutjar un llibre per la seva portada, en biociència no tot és el que sembla; un enfocament creatiu podria ser la clau per fer servir els nostres coneixements, així com els recursos que ens ha ofert l’evolució, en el nostre benefici.
Per saber-ne més
Vall d’Hebron Institut de Recerca (VHIR) – Un estudi amb participació de Vall d’Hebron demostra la seguretat de la teràpia amb virus per combatre bacteris multiresistents
Ciència Oberta – Virus contra bacteris: els bacteriòfags
Ciència Oberta – La fagoteràpia: el tractament soviètic oblidat
Nature – Positive and negative aspects of bacteriophages and their immense role in the food chain
Núvol – Els investigadors no tenen capacitat de pressió social
Sobre l’autora: Laura Arribas Ruscalleda
Graduada en Biologia a la UAB i actualment realitzant la tesi doctoral en Biomedicina a Les Palmes de Gran Canària. La meva vocació investigadora es centra en l’àmbit de la virologia, ja que sempre m’he sentit profundament intrigada a destapar les incògnites que s’amaguen en la biologia viral.
A part de la meva devoció pels virus, em considero una eterna defensora de la divulgació científica, que he promogut participant en La Marató de 3Cat 2023, coordinant els seminaris pre/postdoctorals del meu centre d’investigació i cofundant una compte d’Instagram de divulgació centrada en la virologia (@virologicas), focalitzada a compartir coneixements de virologia amb un llenguatge planer per poder salvar l’escletxa entre els articles científics i una població no tan especialitzada.

Referències
[1] Taylor, M. (2014). Viruses and Man: A History of Interactions. Springer. https://doi.org/10.1007/978-3-319-07758-1_1
[2] Guzmán, M. (2015). El bacteriófago, cien años de hallazgos trascendentales. Biomédica, 35(2), 159–161. https://doi.org/10.7705/biomedica.v35i2.2359
[3] Chanishvili, N. (2014). Phage Therapy—History from Twort and d’Herelle Through Soviet Experience to Current Approaches. In Advances in Virus Research (Vol. 83, pp. 3–40). Academic Press. https://doi.org/10.1016/B978-0-12-394438-2.00001-3
[4] Naghavi, M., et al. (2023). Global burden of bacterial antimicrobial resistance 1990–2021: A systematic analysis with forecasts to 2050. The Lancet, 404(10459), 1199–1226. https://doi.org/10.1016/S0140-6736(23)01329-7
[5] Hendrix, R. (2002). Bacteriophages: Evolution of the Majority. Theoretical Population Biology, 61(4), 471–480. https://doi.org/10.1006/tpbi.2002.1590
[6] Hendrix, R. (1999). Evolution: The long evolutionary reach of viruses. Current Biology, 9(19), 914–917. https://doi.org/10.1016/S0960-9822(00)80103-7
[7] Glonti, T., & Pirnay, J.-P. (2022). In Vitro Techniques and Measurements of Phage Characteristics That Are Important for Phage Therapy Success. Viruses, 14(7), 1490. https://doi.org/10.3390/v14071490
[8] Dedrick, R., Smith, B., Cristinziano, M., Freeman, K., Jacobs-Sera, D., Belessis, Y., … Hatfull, G. (2023). Phage Therapy of Mycobacterium Infections: Compassionate Use of Phages in 20 Patients With Drug-Resistant Mycobacterial Disease. Clinical Infectious Diseases, 76(1), 103–112. https://doi.org/10.1093/cid/ciac453
[9] Little, J., Dedrick, R., Freeman, K., et al. (2022). Bacteriophage treatment of disseminated cutaneous Mycobacterium chelonae infection. Nature Communications, 13, Article 1690. https://doi.org/10.1038/s41467-022-29689-4
[10] Strathdee, Steffanie A. et al. (2023) Phage therapy: From biological mechanisms to future directions. Cell, Volume 186, Issue 1, 17 – 31. https://doi.org/10.1016/j.cell.2022.11.017
Imatge 2: Extreta de “Global burden of bacterial antimicrobial resistance 1990–2021: a systematic analysis with forecasts to 2050”. Naghavi, Mohsen et al. The Lancet, Volume 404, Issue 10459, 1199 – 1226 https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(24)01867-1
Revisors: Pau Clavell Revelles, Mar Barrantes Cepas, Victor Naharro Oriol