Quan parlem de càncer, una de les coses que hem de tenir clara és que és un conjunt de malalties extremadament complex. El fet que amb el temps desenvolupem un càncer o, pel contrari, n’estiguem protegits, depèn en gran mesura de factors externs –com ara la dieta. Alhora, però, una correcta disposició dels elements del mateix organisme –com ara la genètica– també pot ser decisiva per impedir-lo.
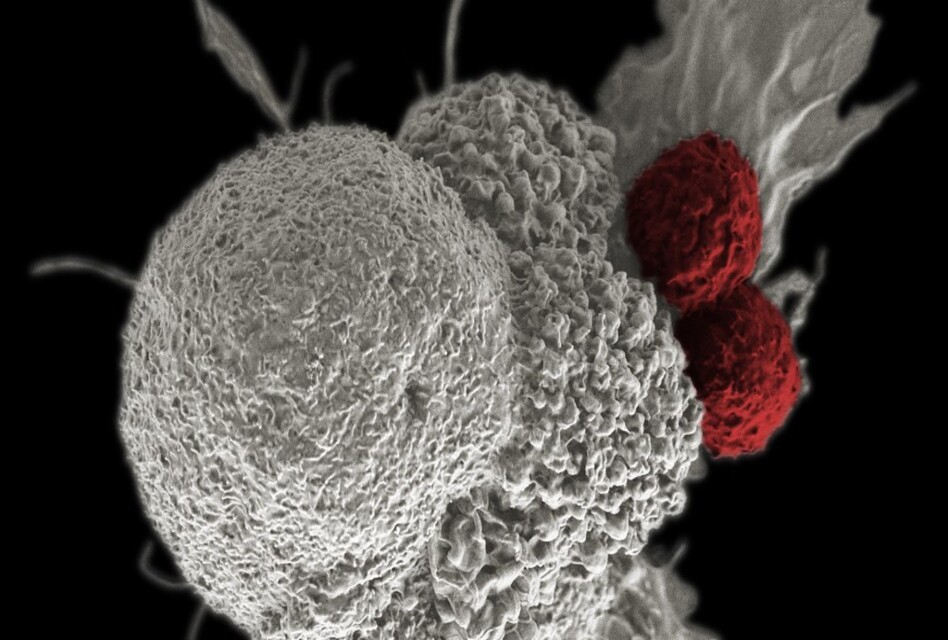
En aquest sentit, hem de saber que el sistema immunitari –aquell encarregat d’identificar i respondre davant d’agents “estranys” potencialment perjudicials– juga un rol molt important no només en la iniciació i progressió del càncer, sinó també en la metàstasi. De fet, una resposta immune natural és crucial per preveure el creixement i evolució d’un tumor. Així, avui explorem la relació entre el càncer i immunitat per entendre com constitueix un gran punt de partida per a les anomenades immunoteràpies.
El tumor, aquella versió maligna de les nostres cèl·lules, davant el sistema immunitari
Com ja hem dit, el sistema immunitari porta a terme un reconeixement i un procés d’eliminació de tot element que no reconeix com a propi. Això pot ser tant un virus o un bacteri durant una infecció, com una cèl·lula cancerosa o una cèl·lula que es divideix descontroladament. Però com conciliem el fet que un tumor, sorgit del propi organisme, sigui reconegut com una entitat aliena?
El tumor presenta elements reconeguts com a estranys
Pràcticament totes les cèl·lules del nostre cos presenten petites molècules de proteïna (pèptids) a la seva superfície que poden actuar com a antígens. Aquests pèptids poden provenir de la degradació de proteïnes pròpies o, en cas d’infeccions, de virus i bacteris. A mode d’escàners, les cèl·lules del sistema immune tenen receptors a la superfície que poden reconèixer aquests antígens específicament –com si fos el codi de barres de les cèl·lules– per desencadenar una resposta i eliminar potencials amenaces. És clar, el nostre sistema immunitari té mecanismes per no reaccionar davant d’antígens propis i, així, evitar atacs al nostre propi cos en condicions normals (mecanismes que, en malalties autoimmunes, fallen).
Però tornem al tumor. En teoria, les cèl·lules tumorals també presenten pèptids a la seva superfície. Podríem pensar que, de la mateixa manera que en la resta, no hauria d’haver-hi cap resposta perquè els pèptids són propis. I és veritat, però fins a cert punt. El càncer és una malaltia en què es requereixen i produeixen moltíssimes alteracions genètiques. És a dir, les mutacions en el DNA poden acabar alterant la composició de les proteïnes –i per extensió, el seu funcionament normal. Això provoca que es generin nous pèptids diferents dels normals: els neoantígens. El sistema immune ja no identifica el codi de barres com a nostre i es pot donar una resposta immunitària contra el tumor.
Un cicle que evita el creixement dels tumors
El procés pel qual el sistema immune ataca a un tumor, doncs, es pot resumir en un cicle de 7 etapes: és el cicle d’immunitat contra el càncer. A través d’aquest, es pot entendre com el sistema immune aprèn a identificar el tumor i com executa i amplifica la seva resposta anti-tumoral.
Quan una cèl·lula cancerosa mor, els potencials neoantígens s’alliberen a l’exterior i són captats per les anomenades cèl·lules presentadores d’antígens. Aquestes cèl·lules recullen i processen els antígens per després migrar als nòduls limfàtics, on entrenaran a cèl·lules immunes (principalment limfòcits T i B). Hem d’entendre els nòduls limfàtics com centres que arrepleguen tot el catàleg d’antígens disponibles per entrenar i programar una resposta immunitària (o no) i supervisar que les diverses parts del cos estan bé; més o menys com fer inventari i fer que tots els escàners funcionin com cal. Així doncs, té lloc una exposició de les cèl·lules immunes als antígens tumorals. Les que tinguin capacitat d’identificar-los, podran ser seleccionades i activades. Un cop entrenades, viatgen cap al tumor on, ara sí, el reconeixement específic dels neoantígens les activa per matar a les cèl·lules canceroses. I així, el cicle pot tornar a començar.
Aquesta supervisió immune del càncer és un mecanisme molt important que funciona fins i tot quan altres mecanismes supressors de tumors han fallat en frenar la malaltia.
Quan el sistema immune no pot reconèixer el càncer: l’evasió immune
La realitat és que, tot i que el sistema és eficient i funciona en molts casos, el cicle es veu truncat en els pacients de càncer. Això es coneix com l’evasió de la supervisió immune, i és considerat com una de les principals característiques que defineixen el càncer.
Així doncs, les cèl·lules tumorals desenvolupen mecanismes per evitar o frenar l’acció del sistema immune. Això fa que només aquestes puguin seguir creixent per un efecte que anomenem de pressió selectiva –la immunitat mata les cèl·lules susceptibles, i les que no ho són queden sense poder identificar-se– i que el tumor, en conjunt, arribi a un estat més esmunyedís.
Aquesta evasió es pot produir per diferents mecanismes. Principalment, es dona una manca de reconeixement d’antígens, ja sigui perquè no es presenten a la superfície o perquè els mecanismes per obtenir els pèptids no funcionen. A més, les cèl·lules tumorals poden expressar inhibidors de les cèl·lules immunes o evitar que aquestes arribin al tumor a combatre’l, així com expressar molècules que eviten la mort cel·lular que provoquen. Un altre factor important és la producció d’altres molècules inhibidores i el reclutament de cèl·lules immunes supressores. En definitiva, entre aquests mecanismes –i molts més– es dona un camuflatge del tumor i una fortificació del seu microambient.
I si reactivem l’acció immune? Les immunoteràpies
Amb tot això en ment, les immunoteràpies sorgeixen amb l’objectiu de restablir la immunitat natural i superar les barreres de l’evasió. És clar, és tot un repte, però avui en dia les immunoteràpies es troben en primera línia contra diferents tipus de càncer, com ara melanoma o el càncer de mama, com bé explicava en Pau en aquest article.
A grans trets, les immunoteràpies es poden dividir en tres estratègies. Per una banda, tenim la infusió de cèl·lules immunes modificades dels propis pacients preparades per identificar els tumors; en són un exemple les teràpies amb cèl·lules CAR T. D’altra banda, també es proven vacunes –tant terapèutiques com profilàctiques– amb l’objectiu d’entrenar al sistema immunitari a través de neoantígens produïts pels tumors. Per últim, tenim els inhibidors de punt de control, que tenen l’objectiu d’incentivar l’activació dels limfòcits T contra el càncer a través del bloqueig de les molècules inhibidores que en situacions normals regulen la resposta immune.
Ja per acabar…
Les immunoteràpies han revolucionat el tractament de molts tipus de càncer. Ja sigui en solitari o en combinació amb altres tipus de teràpies, constitueixen una eina molt útil per aprofitar els mecanismes del nostre propi organisme. Tot i que tampoc no estan exemptes d’efectes secundaris (induir una resposta immunitària contra el tumor pot suposar un control menor en les respostes autoimmunes), han provat ser eficients en provocar respostes anti-tumorals duradores i fins i tot, remissions. Tanmateix, ni tots els càncers, ni tots els tipus d’un mateix càncer ni, encara, tots els pacients d’un mateix tipus poden beneficiar-se d’aquestes teràpies. És aquí on entra l’estudi de les característiques que afavoreixen l’acció i el correcte funcionament de les immunoteràpies per predir la resposta; un pas que ens apropa a la medicina personalitzada.
Per saber-ne més
Immunity – Oncology Meets Immunology: The Cancer-Immunity Cycle
National Cancer Institute – Immunotherapy to Treat Cancer
Nature Reviews Immunology – A guide to cancer immunotherapy: from T cell basic science to clinical practice
1. Imatge traduïda i adaptada de Chen, D. S., & Mellman, I. (2013). Oncology Meets Immunology: The Cancer-Immunity Cycle. Immunity, 39(1), 1–10. https://doi.org/10.1016/J.IMMUNI.2013.07.012
2. Imatge feta amb Biorender.com