Als laboratoris on es treballa amb organismes modificats genèticament es prenen mesures per evitar que hi hagi fugues. Tanmateix, el mes passat es van anunciar els resultats d’un assaig on, intencionadament, es van alliberar a la natura cinc milions de mosquits modificats genèticament!
L’objectiu d’aquest estudi era descobrir si les modificacions genètiques fetes als mosquits es transmetien a la descendència tal com es volia. Què tenen d’especial aquests mosquits? Com els hi han alterat el seu material genètic?
Quina utilitat té tot plegat? Aquestes i d’altres preguntes, les respondrem en aquest reportatge.
Uns petits assassins
Els mosquits són responsables de més de 700 mil morts cada any i les estimacions el consideren l’animal més mortífer de la Terra, fins i tot per sobre dels mateixos humans. Encara que les vertaderes culpables són les malalties que transporten, les poblacions de mosquits són imprescindibles per la seva transmissió.

Espècies com Aedes aegypti o espècies pertanyents al gènere Anopheles son vectors transmissor de malalties com el dengue, la febre groga, la malària o el Zika. Per tal d’intentar reduir la incidència d’aquestes malalties, que afecten sobretot zones tropicals, una de les mesures més efectives és reduir la població d’aquests mosquits.
Un cop de mà de la genètica
Això és precisament el que està portant a la pràctica l’empresa biotecnològica britànica Oxitec. Per fer-ho, no han optat per utilitzar verins insecticides ni trampes per a mosquits, sinó que han utilitzat avançades eines d’enginyeria genètica per modificar genèticament mosquits al laboratori. Concretament, la idea ha estat introduir uns gens que provoquin la mort del mosquit abans que es puguin reproduir.
Però, com podem fer que uns mosquits de laboratori introdueixin un gen letal a la població salvatge (per reduir-la) sense que el mateix gen els mati? Per aconseguir aquest objectiu, s’han utilitzat diferents mecanismes aprofitant que només piquen les femelles, i per tant, que són les úniques capaces de transmetre’ns malalties.
Dues estratègies diferents
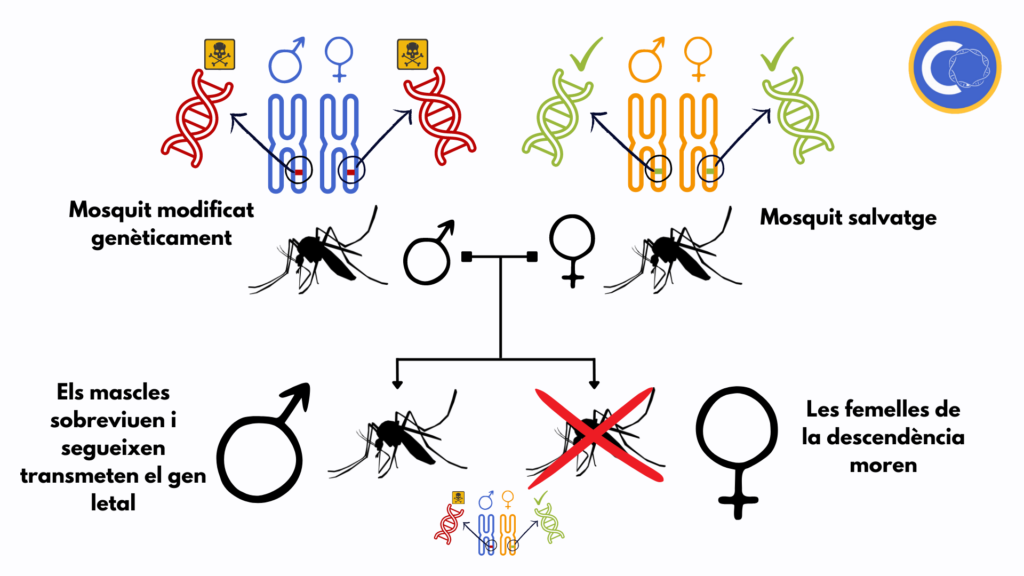
Els científics han optat per dues estratègies diferents. La primera és l’emprada als mosquits de l’assaig d’Oxitec, que han estat modificats genèticament per contenir un gen que acaba matant a les femelles, mentre que els mascles que el tenen poden viure i reproduir-se sense problema. D’aquesta manera, cada vegada hi ha menys femelles en les noves generacions, i els nous mascles poden seguir transmetent el gen letal a la descendència.
L’estratègia d’una altra empresa anomenada MosquitoMate, que també ha pogut fer assajos als Estats Units amb més de 20 milions de mosquits, consisteix en utilitzar un bacteri que infecta els mosquits anomenat Wolbachia. La gràcia d’aquesta infecció és que les larves d’aquest mosquit no arriben a sortir de l’ou si el mascle està infectat i la femella no. Aleshores, alliberant mascles infectats, s’aconsegueix que es reprodueixin amb femelles sanes salvatges i que la descendència no pugui arribar a néixer.
Hi ha problemes importants
Tanmateix, ambdues estratègies tenen el mateix problema i és que al cap d’unes generacions deixen de funcionar. A l’assaig d’Oxitec s’ha vist que arriba un punt en què el gen letal que mata les femelles ja ha desaparegut de la població. Això passa perquè cada còpia d’un gen té una possibilitat d’un 50% que es transmeti a la descendència, de manera que amb el pas de les generacions, la presència d’aquell gen a la població de mosquits es va diluïnt fins a desparèixer.
Pel que fa als mosquits infectats amb Wolbachia de MosquitoMate, l’estratègia deixa de funcionar un cop els mascles infectats ja han anat infectant la població i es troben amb femelles també infectades, ja que llavors, els nous mosquits sí que son viables.
Dirigir l’herència genètica amb CRISPR
En conclusió, cal trobar un mecanisme que faci que l’element que perjudica la reproducció, concretament un gen letal, s’estengui al màxim nombre d’individus de les noves generacions.
Aquí entra en joc l’eina d’enginyeria genètica CRISPR-Cas, una tecnologia que va valer el premi Nobel de Química del 2020 a Jennifer Dounda i Emmanuelle Charpentier i que utilitza com a fonament les seqüències CRISPR descobertes pel valencià Francis Mojica.

L’estratègia basada en CRISPR-Cas9 té una funció molt senzilla que és fer que la còpia del gen letal que al principi només estava al cromosoma patern es copii al matern. Així, s’aconsegueix que els dos cromosomes del mosquit tinguin el gen letal (que només afecta a les femelles) i que per tant, al reproduir-se, el 100% de la descendència d’aquests mosquit l’adquireixi. En aquest nou mosquit el fenomen es repeteix i, així, la descendència sempre té el gen letal i s’expandeix en la població.
Cal matissar que els mosquits modificats que s’han utilitzat a la natura en aquests assajos no conten aquest mecanisme de genètica dirigida amb CRISPR i que, per tant, el gen letal no s’expandeix en la població salvatge.
Com s’obtenen aquests mosquits?
Un altre dels desavantatges d’aquestes estratègies és que cal alliberar una gran quantitat de mosquits, milions, per arribar a tenir un efecte sobre les enormes poblacions naturals. És evident, doncs, que cal obtenir molts mosquits i la dificultat està en modificar-los genèticament. És molt complicat modificar genèticament milions d’organismes, ja que els mecanismes per fer-ho són molt poc eficients, laboriosos i cars.
Per aquest motiu, el més intel·ligent és fer que els mosquits amb el gen letal es reprodueixin sols perquè creïn més mosquits! Aquesta lògica és tan evident com absurda en el moment en què parlem de mosquits amb afectacions que impossibiliten la reproducció. Però afortunadament, hi ha una solució que és fer que el gen letal quedi completament inactivat en la presència d’un compost químic anomenat tetraciclina. Podem barrejar aquesta tetraciclina, que també s’utilitza com a antibiòtic, amb el seu aliment en el laboratori, per fer que els mosquits procreein i se’n puguin obtenir a gran escala.
Les properes passes en el camp
En aquest primer estudi d’Oxitec s’ha vist que el gen letal arriba correctament a la població salvatge, encara que al cap d’unes generacions acabi desapareixent, ja que no disposa de la tecnologia de genètica dirigida amb CRISPR. El proper assaig, que ja ha estat aprovat per l’Agència de Protecció Mediambiental del Estats Units (EPA), preveu alliberar una quantitat molt més gran de mosquits per analitzar la capacitat del mecanisme per reduir la població salvatge.
Ja per acabar…
A nivell metodològic, durant l’estudi ha estat necessari distingir mosquits i larves amb el gen letal o sense el gen. Per fer-ho s’ha utilitzat un gen que genera una proteïna fluorescent d’un color taronjós que es transmet juntament amb el gen letal. Així, quan es troba una larva fluorescent (mentre s’irradia amb una llum concreta) es pot concloure que conté el gen letal, fet fonamental per fer un seguiment de l’evolució de la població de mosquits transgènics.
Per saber-ne més
Nature – Biotech firm announces results from first US trial of genetically modified mosquitoes
Ciència Oberta – La genètica dirigida
Ciència Oberta – Per què ens piquen els mosquits?
- Obtingut de Wikimedia Commons